您现在的位置是: 首页 > 高考动态 高考动态
江苏省高考化学题,江苏高考答案化学
tamoadmin 2024-05-16 人已围观
简介1.求:江苏省南京市2008—2009学年度高三第一学期期末调研测试卷 化学的试题和答案这题可以用两种方法:1、由于乙烯和丁烯的最简式都是CH2,所以混合物含碳量始终为21*12/14=18g,即含有的碳原子物质的量=18/12=1.5mol,碳原子数为1.5NA 。2、用极端思维法设21.0g都是乙烯,那么物质的量=21/28=0.75mol,含碳物质的量=0.75*2=1.5mol,碳原子数为
1.求:江苏省南京市2008—2009学年度高三第一学期期末调研测试卷 化学的试题和答案
这题可以用两种方法:
1、由于乙烯和丁烯的最简式都是CH2,所以混合物含碳量始终为21*12/14=18g,即含有的碳原子物质的量=18/12=1.5mol,碳原子数为1.5NA 。
2、用极端思维法
设21.0g都是乙烯,那么物质的量=21/28=0.75mol,含碳物质的量=0.75*2=1.5mol,碳原子数为1.5NA ;再设21.0g都是丁烯,那么物质的量=21/56=0.375mol,含碳物质的量=0.375*4=1.5mol,碳原子数为1.5NA ,所以乙烯和丁烯的混合气体一定含碳原子数1.5NA
求:江苏省南京市2008—2009学年度高三第一学期期末调研测试卷 化学的试题和答案
[Zn(NH3)4]cl2中的化学键类型为:
[Zn(NH3)4]2+ 与Cl-之间为离子键,所以含有共价键的只有[Zn(NH3)4]2+内部了:
1、Zn←N
4mol σ 配键
2、N-H
3* 4 = 12 mol σ 键
所以,每1mol的[Zn(NH3)4]2+中一共有 σ 键4+12 = 16mol(16NA)
其中配位键有4 mol(4NA)
你好
可能用到的相对原子质量:H—1 C—12 O-16 Mg-24 Al-27
第I卷(选择题.共48分)
一、单项选择题(本题包括8小题,每小题3分.共24分。每小题只有一个选项符合题意)
1.在2008年春节期间,许多遭受雪灾的地区使用融雪盐除雪。下列有关说法不正确的是
A.融雪盐能使盐水混合物的凝固点降低
B.融雪盐只能使用氯化钠
C.过量使用融雪盐会加速钢铁桥梁的腐蚀
D.撒了融雪盐的积雪不宜往绿地、河流中倾倒
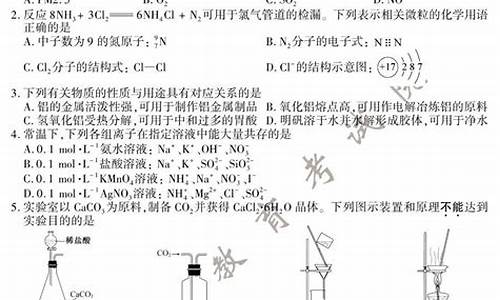
2.下列说法正确的是
A.淀粉和纤维素的组成都可用(C6H10O5)n表示,它们互为同分异构体
B.CH2=CHC(CH3)3与氢气完全加成后,生成物的名称是3,3-二甲基丁烷
C.CS2的结构式为S=C=S
D.一CH3(甲基)的电子式为
3.下列说法不正确的是
A.根据沸点差异可以判断两种液体混合物是否可用蒸馏方法进行分离
B.根据固体溶解度曲线可以判断物质结晶的方法
C.根据熵变可以判断所有化学反应能否自发进行
D.根据化学平衡常数可以判断化学反应进行的限度
4.生活中常用到一些化学知识,下列分析中正确的是
A.医疗上可用硫酸钡作x射线透视肠胃的内服药,是因为硫酸钡不溶于水
B.氯气可用作消毒剂和漂白剂,是因为氯气与水反应生成的次氯酸具有强氧化性
C.某雨水样品放置一段时间后pH由4.68变为4.28,是因为水中溶解的CO2增多
D.加碘食盐中添加碘酸钾而不用碘化钾,是因为碘酸钾能溶于水而碘化钾不溶于水
5.下列说法正确的是
A.在周期表中金属与非金属的分界处可以找到半导体材料
B.H2S、H2Se、HF的热稳定性依次增强
C.NaOH、KOH、Mg(OH)2的碱性依次减弱
D.Cl、S、N元素的非金属性依次增强
6.下列实验能达到预期目的的是 ①用乙醇和浓硫酸除去乙酸乙酯中混有的少量乙酸 ②用NaOH溶液除去苯中混有的少量苯酚 ③用饱和NaHCO3溶液除去CO2中混有的少量HCl ④用加热的方法提取NH4Cl固体中混有的少量碘 ⑤用食醋和澄清石灰水验证蛋壳中含有碳酸盐
⑥用碘酒验证汽油中含有不饱和烃
A.①②④⑤⑥ B.②③⑤⑥ C.②③④⑤D.①②③④⑤⑥
7.A是一种常见的单质,B、C为常见的化合物,A、B、C均含有元素x,它们有如图所示的转化关系(部分产物及反应条件已略去)。下列说法中正确的是
A.X元素可能为铝
B.反应①和②互为可逆反应
C.X元素可能是金属,也可能是非金属
D.反应①和②一定为氧化还原反应
8.下列各组物质中.气体X和气体Y在通常条件下同时通入盛有溶液z的洗气瓶中(如右下图
所示),一定没有沉淀生成的是
X Y Z
A NO2 SO2 BaCl2
B NH3 O2 Al2(SO4)3
C NH3 CO2 NaCl(饱和)
D CO O2 Ca(OH)2
二、选择题(本题包括6小题,每小题4分,共24分。每小题有一个或二个选项符合题意。若正确答案包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分)
9.咖啡鞣酸具有较广泛的抗菌作用,结构简式如图所示:下列关于咖啡鞣酸的说法,不正确的是
A.分子式为C16H18O9
B.在一定条件下能发生消去反应
C.1 mol咖啡鞣酸水解时可消耗8 mol NaOH
D.与浓溴水既能发生取代反应又能发生加成反应
10.阿伏加德罗常数为6.02×1023mol-1,下列说法正确的是
A.1 mol HClO完全分解时转移电子数为2×6.02×1023
B.a L O2和N2的混合物中含有的分子数为a/22.4 ×6.02×1023
C.100 mL 0.1 mol/L的Al2(SO4)3溶液中含有的Al3+数目为0.02×6.02×1023
D.常温下,42 g C2H4和C4H8的混合物中含有的碳原子数为5×6.02×1023
11,下列化学反应的离子方程式正确的是
A.向Ba(OH)2溶液中滴加NH4HSO4。溶液至刚好沉淀完全:
Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+H2O
B.苯酚钠溶液通入二氧化碳气体:2C6H5O-+CO2+H2O=2C6H5OH十CO32-
C.将少量SO2气体通入足量的NaClO溶液中:SO2+2ClO-+H2O=SO32-+2HClO
D.稀硝酸中加入过量的铁屑:3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O
12.下述实验能达到预期目的的是
编号 实验内容 实验目的
A 向蔗糖溶液中加入4滴稀硫酸,煮沸几分钟、冷却,再加入银氨溶液,水浴加热 检验蔗糖是否已水解
B 将Cl2通入NaBr溶液中 比较氯气与溴的氧化性强弱
C 将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却降温 研究温度对化学平衡的影响
D 分别向2支试管中加入相同体积不同浓度的H2O2溶液,再向其中1支加入少量MnO2 研究催化剂对H2O2分解速率的影响
13.T℃时,将气体X与气体Y置于一密闭容器中,反应生成气体Z,反应过程中各物质的浓度变 化如图(I)所示。保持其他条件不变,在T1、T2两种温度下,Y的体积分数变化如图(Ⅱ)所示。下列结论正确的是
A.t2时,保持其它条件和物质状态不变,增加压强,化学平衡向逆反应方向移动
B.T℃时,若密闭容器中各物质起始浓度为:0.4 mol/L X、0.4 mol/L Y、0.2 mol/L Z。保持其他条件不变,达到平衡时z的浓度为0.4 mol/L
C.图(Ⅱ)中T1>T2,则正反应是吸热反应
D.其他条件不变,升高温度,正、逆反应速率均增大,且X的转化率增大
14.下列叙述正确的是
A.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2] < c[(NH4)2SO4] < c(NH4Cl)
B.向AgCl悬浊液中滴入KI溶液,有AgI沉淀生成,说明AgCl的溶解度小于AgI的溶解度
C.0.2 mol/L HCl溶液与等体积0.05 mol/L Ba(OH)2溶液混合后,溶液的pH=1
D.0.2 mol/L的NaHCO3溶液中c(H+)+c(H2CO3)=c(CO32-)+c(OH-)
第II卷 (非选择题共72分)
三、(本题包括1小题,共10分)
15.(10分)铜是重要的金属材料。
(1)工业上可用Cu2S和O2反应制取粗铜,该反应中氧化剂为 ▲ 。电解粗铜制取精铜,电解时.阳极材料是 ▲ ,电解液中必须含有的阳离子是 ▲ 。
(2)在100 mL 18 mol/L浓硫酸中加入过量的铜片,加热使之充分反应,反应中被还原的
H2SO4< ▲ mol。
(3)电子工业曾用30%的FeCl3溶液腐蚀敷有铜箔的绝缘板制印刷电路板,为了从使用过的废腐蚀液中回收铜,并重薪得到FeCl3溶液,设计如下实验流程。
上述流程中,所加试剂的化学式为:X ▲ ,Y ▲ Z ▲ ;第⑥步反应的离子方程式为 ▲ 。
四、(本题包括1小题,共10分)
16.(10分)化学在能源开发与利用中起着十分关键的作用。
(1)蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体。甲烷气体燃烧的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3 kJ/mol。
356g“可燃冰”(分子式为CH4·9H2O)释放的甲烷气体完全燃烧生成液态水.放出的热量为 ▲ 。
(2)某种燃料电池,一个电极通入空气,另一电极通入液化石油气(以C4H10表示),电池的电解质是掺入了Y2O3的ZrO2晶体,它在高温下传导O2-。
已知该电池负极的电极反应为:C4H10+2O2--4e-=CO2+H2O,则该电池正极的电极反应式为 ▲ ,电池工作时,固体电解质里的O2-向 ▲ 极移动。
(3)已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g) CO2(g)+H2(g)
①T℃时,在一定体积的容器中,通入一定量的CO(g)和H2O(g),发生反应并保持温度不变,各物质浓度随时间变化如下表: T℃时物质的浓度(mol/L)变化
时间 / min CO H2O(g) CO2 H2
0 0.200 0.300 0 0
2 0.138 0.238 0.062 0.062
3 0.100 0.200 0.100 0.100
4 0.100 0.200 0.100 0.100
5 0.116 0.216 0.084 C1
6 0.096 0.266 0.104 C2
第5、6min时的数据是保持温度和体积不变时,改变某一条件后测得的。第4~5min之间,改变的条件是 ▲ ,第5~6min之间,改变的条件是 ▲ 。T℃时该化 学反应的平衡常数是 ▲ 。
②已知420℃时,该化学反应的平衡常数为9。如果反应开始时,CO和H2O(g)的浓度都是0.01 mol/L,则CO在此条件下的转化率为 ▲ 。
③397℃时该反应的平衡常数为12,请判断该反应的△H ▲ 0(填“>”、“=”、“<”).
五、(本题包括l小题,共12分)
17.(12分)实验室用右图所示的装置制取溴乙烷。在试管I中依次
加入2 mL 蒸馏水、4 mL浓硫酸、2 mL 95%的乙醇和3g溴化钠
粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水。加热试管
I至微沸状态数分钟后,冷却。
试回答下列问题:
(1)试管I中浓硫酸与溴化钠加热反应生成氢溴酸,写出氢溴酸与乙醇在加热时反应的化学方程式 ▲ 。
(2)试管I中反应除了生成溴乙烷,还可能生成的有机物有 ▲ (任写两种结构简式)。
(3)设计实验证明试管Ⅱ收集的溴乙烷中含有溴元素,完成以下实验报告:
实验步骤 实验操作 预期现象和结论
1 ▲ ▲
2 ▲ ▲
3 ▲ ▲
4 ▲ ▲
(4)设计实验方案,检验溴乙烷与NaOH乙醇溶液发生消去反应后生成的气体X中是否含乙烯。在答题卡对应的方框中画出实验装置图,并注明所用试剂的名称。
六、(本题包括1小题,共8分)
18.(8分)80年代中期美国学者Modell首次提出超临界水氧
化技术(SCWO)。超临界流体(SCF)是指流体的温度和压
力处于它的临界温度(Tc)和临界压力(Pc)以上时的一种
特殊状态的流体,它具有许多独特的性质,如无机盐在超
临界水(SCW)中的溶解度很低。水的状态与压强、温度的
关系如右图。
(1)在380℃.20 MPa时,水的状态是 ▲ ,若要使
之成为超临界水,必须采取的措施是 ▲ 。
(2)以超临界水为介质,用氧气等氧化剂可将有机废物氧化成二氧化碳、氮气、水等无毒小分子。在超临界水中,偏二甲胼[(CH3)2NNH2]能迅速被H2O2氧化,写出该反应的化学方程式:
▲
(3)SCWO基本工艺流程如下图所示:
利用以上工艺流程处理某些含可溶性无机盐(只含钠盐、钾盐)的有机废水时,常常会出现管道堵塞现象,发生这种现象的原因是 ▲ 。若检测到管道c中的流体的温度为287℃,管道e、d中的流体的温度为227℃,则上述a~h管道中易发生堵塞的管道为 ▲ (填字母)。
七、(本题包括1小题,共11分)
19,(11分)维生素C(分子式为C6H8O6)可预防感染、坏血病等。其工业合成路线如下图所示:
I.(1)上述①~③反应中,属于加成反应的有 ▲ (填数字序号)。
(2)A~G七种物质中与C互为同分异构体的有 ▲ (填字母序号)。
(3)比较D和G的结构可知,G可看成由D通过氧化得到。工业生产中在第⑤步氧化的前后设计④和⑥两步的目的是 ▲ 。
(4)H的结构简式是 ▲ 。
Ⅱ.已知,
利用本题中的信息,设计合理方案由 (用反应流程图表示,
并注明反应条件)。 ▲
例:由乙醇合成聚乙烯的反应流程图可表示为
八、(本小题包括1小题,共9分)
20、(9分)某研究性学习小组为测定镁和铝的混合物中铝的质量分数,称取该混合物a g,溶于200 mL 5 moL HCl溶液中,共收集到标准状况下的氢气3.36 L。
(1)a的取值范围是 ▲ 。
(2)向反应后所得溶液中逐渐加入4 mol/L的NaOH溶液。当沉淀质量达到最大值时,加入的NaOH溶液的体积是 ▲ mL,沉淀的最大质量是 ▲ g(用含a的代数式表示)
(3)继续加入NaOH溶液至沉淀质量不再发生变化时,过滤、洗涤并灼烧沉淀至恒重,所得残余固体的质量仍为a g,计算原混合物中铝的质量分数(写出计算过程)。
九、(本题分A、B两题,考生只要选择其中一题作答。若两题都作答,则以A题得分计入总分。本题共12分。)
2l A.《物质结构与性质》(12分)
(1)前三周期元素中第一电离能最小的是 ▲ (填元素符号),其基态原子的电子排布式为 ▲ 。第二周期非金属元素形成的氢化物中化学键极性最大的是 ▲
(填分子式),该物质在CCl4中的溶解度比在水中的溶解度 ▲ (填“大”或“小”)。
(2)物质形成分子间氢键和分子内氢键对物质性质的影响有显著差异。根据下表数据,形成分子间氢键的物质是 ▲ (填物质字母代号)。
(3)晶格能的大小:MgO ▲ NaCl,键能的大小:HBr ▲ HI。(填“>”、“=”或“<”)
(4)下列物质的熔点高低顺序,正确的是 ▲
A.金刚石>晶体硅>二氧化硅>碳化硅
B.CI4 > CBr4 > CCl4 > CH4
C.SiF4 > NaF > NaCl > NaBr
21 B。《实验化学》(12分)
七水硫酸镁(MgSO4·7H2O)在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣-一硼镁泥可制取七水硫酸镁。硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等)。
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
沉淀物 Al(OH)3 Fe(OH)3 Fe(OH)2 Mn(OH)2 Mg(OH)2
pH值 5.2 3.2 9.7 10.4 11.2
表2 两种盐的溶解度(单位为g/100g水)
温度 / ℃ 10 30 40 50 60
CaSO4 0.19 0.21 0.21 0.20 0.19
MgSO4·7H2O 30.9 35.5 40.8 45.6 /
硼镁泥制取七水硫酸镁的工艺流程如下:
根据以上流程图并参考表格pH数据和溶解度数据,试回答下列问题:
(1)过滤I的滤液中加入硼镁泥,调节溶液的pH=5~6,再加入NaClO溶液加热煮沸,将溶液中的Mn2+氧化成MnO2,反应的离子反应方程式为 ▲ 。加热煮沸的主要目的是_ ▲ 。
(2)沉淀B中除MnO2、SiO2外还含有 ▲ (填化学式)等物质。
(3)检验过滤Ⅱ后的滤液中是否含有Fe3+的实验方法是 ▲ ;
(4)沉淀C的化学式是 ▲ 。过滤II需趁热过滤的理由是 ▲
答案
1、B 2、C 3、C 4、B 5、A 6、B 7、D 8、D 9、C 10、AD 11、A 12、BC 13、B 14、AD
15、(1)Cu2S O2 粗铜 Cu2+(每空1分)
(2)0.9(2分)(3)Fe HCl Cl2 2Fe2++Cl2=2Fe3++2Cl-(方程式2分,其余每空1分)
16、(1)1780.6 kJ (2)O2+4e-=2O2-(1分) 负(1分)
(3)增加H2浓度(1分)增加H2O(g)浓度(1分) 0.5(1分) 75%(2分) <(1分)
17(1)C2H5OH+HBr=C2H5Br+H2O(2分)
(2)CH2=CH2(1分) CH3CH2OCH2CH3(1分)其他合理答案也给分
(3)1、取少许试管I中收集的有机物于小试管中,加入NaOH溶液,振荡,加热,静置。
液体分层,上层可能含有NaOH及NaBr
2、取上层清夜于小试管中,加入过量的稀硝酸酸化。无明显现象
3、取少许酸化后的溶液用pH试纸检验。pH试纸呈红色,溶液呈酸性
4、向上述酸化的溶液中滴加AgNO3溶液,有淡**沉淀,溶液中含有Br-,即原有机物中含有Br元素(每步1分共4分,其他合理答案给分)
(4)如下图(装置图2分,试剂2分,共4分。其他合理答案均给分)
18、(1)气体(2分)加压至22MPa以上(1分)
(2)(CH3)2NNH2+8H2O2==2CO2+12H2O+N2
(3)钠盐、钾盐在超临界水中的溶解度很低,易析出固体(2分) f (1分)
19、I (1) 1 3 (2)A、D (3)保护D分子中其他羟基不被氧化
(4)
II
20、(1) 2.7<a<3.6(2分) (2)250 a+5.1
(3)a g 残余固体为MgO(1分)
其中Mg元素的质量为a g × 24/40 =0.6a g (1分)
Al的质量分数=(a g-0.6a g)/a g ×100%=40%(1分)
21A、(1)Na 1S22S22P63S1 HF 小 (各1分)
(2)B 2分 (3)> > 各2分 (4)B (2分)
22B、(1)Mn2++ClO-+H2O=MnO2↓+2H++Cl-(2分)
促进Al3+、Fe3+水解及Mn2+氧化成MnO2(2分)
(2)Fe(OH)3(1分) Al(OH)3(1分)
(3)取过滤II后的滤液1~2 ml于试管中,加入少量KSCN溶液,如果溶液不显红色,证明滤液中无Fe3+(2分)
(4分)CaSO4·2H2O或CaSO4(2分) 以防MgSO4在温度低时结晶析出。
有些 传不上来 你想要百度HI说吧
下一篇:宝坻高考考点,宝坻高考2017